Acerca de los tumores desmoides
Descripción general de la enfermedad:
Una enfermedad infiltrativa y agresiva1
- Los tumores desmoides son tumores localmente agresivos y potencialmente mórbidos de los tejidos blandos, con tendencia a infiltrarse en las estructuras circundantes y extenderse por los planos y los músculos1,2
- A veces denominados fibromatosis agresiva o fibromatosis desmoide,3 estos tumores mesenquimatosos pueden ser graves, debilitantes y, en casos infrecuentes, incluso causar daños orgánicos potencialmente mortales2,4
- Los tumores desmoides pueden infiltrarse en el tejido circundante, comprimiendo músculos, nervios y vasos5,6
Sintomatología y localizaciones tumorales
Los tumores desmoides pueden causar morbilidades graves y debilitantes2
- La sintomatología relacionada con los tumores desmoides varía en función de la localización de la presentación del tumor4,6
- Un estudio prospectivo de cohortes halló que los tumores de la pared torácica, las extremidades superiores y la cabeza y el cuello se asociaban con malos resultados después de la cirugía7
| LOCALIZACIÓN DEL TUMOR | FRECUENCIA ESTIMADA6 | SÍNTOMAS Y COMPLICACIONES COMUNES |
|---|---|---|
| Intraabdominal (including mesentery) | 20% | La compresión puede causar dolor, caquexia, malestar, distensión abdominal u obstrucción de los intestinos o de los uréteres6,8 |
| Pared Abdominal | 16% | Los tumores de gran tamaño pueden provocar estiramiento de los tejidos, compresión de los vasos sanguíneos y desplazamiento del intestino o de la vejiga9 |
| Extremidades Inferiores | 16% | Movilidad limitada, dolor, rigidez muscular o deformidad6,10 |
| Pared Torácica | 15% | Disnea,6 disfagia,6 invasión pleural,8 fectación de la columna vertebral11 o de las costillas,12 erosión ósea,12 y dolor12 |
| Extremidades Superiores | 14% | Movilidad restringida, afectación de músculos y ligamentos, debilidad del miembro, deformidad o dolor6,13 |
| Cabeza Y Cuello | 8% | Dolor, déficit neurológico, proximidad a estructuras vitales, incluido el riesgo de mortalidad por compromiso vascular o de las vías respiratorias14 |
| Otros | 11% | Síntomas y complicaciones dependientes de la localización4,6 |
La ubicación de los tumores desmoides puede afectar significativamente a la calidad de vida.15 Por ejemplo, un tumor desmoide con crecimientos “similares a tendriles”1 que rodean los nervios puede estar asociado a dolor neuropático debilitante.6,16
Evolución de la enfermedad
Variable e impredecible1
- Los tumores desmoides se caracterizan por una evolución variable e impredecible de la enfermedad dependiendo de la localización del tumor y de la morbilidad asociada1,6
- Aproximadamente, el 50 % de los desmoides presentan una biología agresiva, continuando su crecimiento o volviéndose sintomáticos. La gran mayoría de las progresiones (89 %) se produjeron en los primeros 2 años de observación5
Evolución clínica de los tumores desmoides
*El 10–28 % de los tumores desmoides se resolverán espontáneamente sin tratamiento17
Incidencia y factores de riesgo
Epidemiología
El tumor desmoide tiene una incidencia de aproximadamente 5 casos por cada millón de habitantes al año.18
La serie de informes Orphanet proporciona una incidencia anual media de 3 casos de tumores desmoides por millón de años-persona en Europa.17
Los estudios epidemiológicos revelan que la mayoría de los casos de tumores desmoides aparecen en el intervalo de edad de 20 a 44 años.17
- Los tumores desmoides son infrecuentes en personas jóvenes y adultos de edad avanzada.19
- La estimación de la incidencia ha aumentado en los últimos años, lo que puede estar relacionado con una mejora en las técnicas diagnósticas17
Sexo femenino
La proporción entre mujeres y hombres es de aproximadamente 2-3:1.20
- El embarazo puede promover tumores desmoides5
Traumatismo antecedente
Alrededor del 25 % de los pacientes con tumores desmoides tienen antecedentes de traumatismos.6
- Las lesiones o la cirugía pueden aumentar el riesgo21
Mutaciones del APC (gen de la poliposis adenomatosa coli)
Las características fenotípicas se correlacionan con la posición de la mutación del APC en relación con determinados codones.22
- Los pacientes con poliposis adenomatosa familiar (PAF) tienen un riesgo 1000 veces mayor de desarrollar tumores desmoides que la población general20
Etiología y patogénesis de los tumores desmoides
Comprender la patogenia molecular es de gran interés en esta enfermedad, dada su gran variabilidad en su evolución clínica19
- Se cree que la patogénesis de los tumores desmoides está relacionada con un traumatismo5
- a veces la cirugía puede promover el crecimiento del tumor5
- factores de crecimiento liberados después de la cirugía, durante la fase inicial de la cicatrización de heridas, podrían transmitir señales que promueven la activación de la β-catenina5
- El embarazo puede promover el TD no solo secundario a las influencias hormonales, sino también a la liberación sistémica de factores de crecimiento5
- Se han implicado dos vías en la vía canónica Wnt/β-catenina/APC, en la que las mutaciones en los genes CTNNB1 y APC provocan la acumulación de β-catenina, y la vía Notch, en la que se producen dos escisiones en los receptores de Notch 17
- Se cree que la posible interferencia entre las vías de Notch y Wnt, así como la activación de la vía Notch resultante de la desregulación de la vía Wnt, están implicadas en la patogénesis de los tumores desmoides17
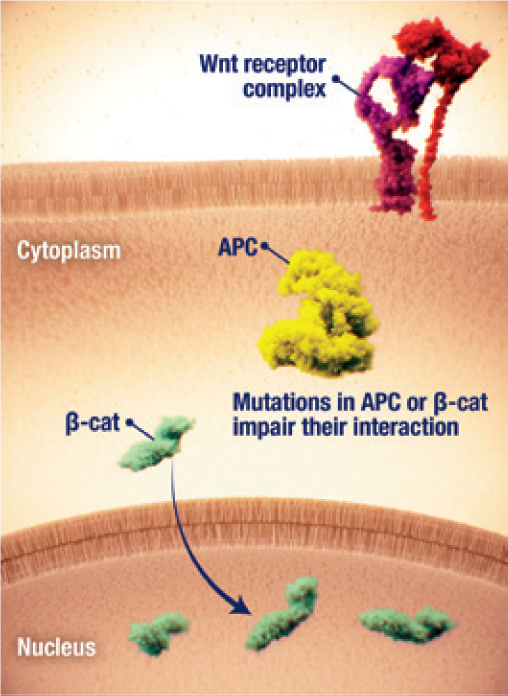
Acumulación nuclear de β-catenina
- La desregulación de la vía Wnt/β-catenina se ha relacionado con la patogénesis de los tumores desmoides2,23
- La acumulación nuclear de β-catenina y la subsiguiente transcripción génica son un factor clave que impulsa la proliferación de células tumorales desmoides2,24
- La acumulación nuclear de β-catenina puede iniciarse por2,24
- Mutaciones activadoras del gen de la β-catenina CTNNB1
- Mutaciones inactivadoras en el APC regulador negativo, a menudo en poliposis adenomatosa familiar (PAF)
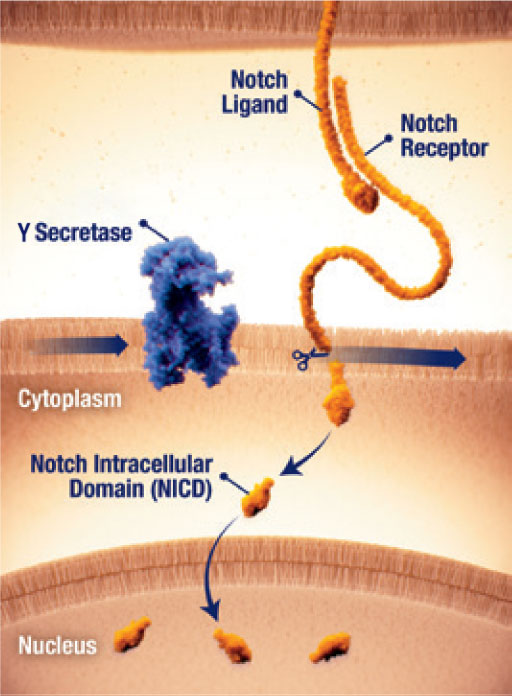
Activación de Notch por la γ-secretasa
- La vía Notch puede estar activa en los tumores desmoides25
- Cuando se desregula, Notch puede activar vías que contribuyen al crecimiento tumoral25
- La señalización del receptor de Notch requiere la activación proteolítica por la enzima γ-secretasa (gamma secretasa)25
- La escisión de la γ-secretasa libera el dominio intracelular de Notch (DICN), que se transloca al núcleo y activa la transcripción génica25
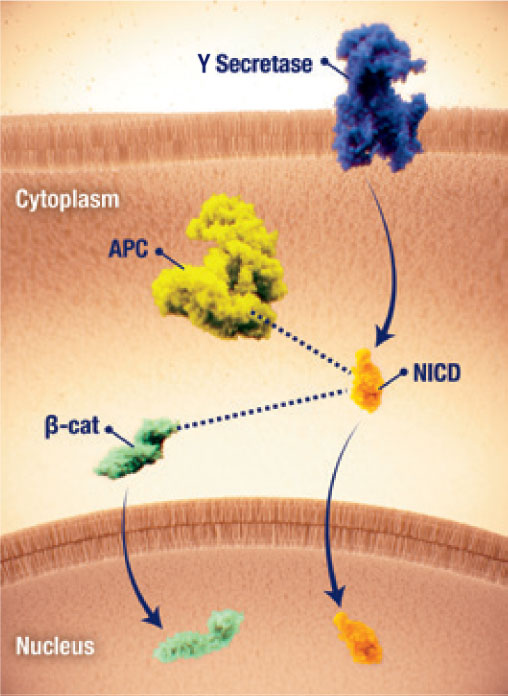
Intercomunicación de la vía
- La interferencia entre las vías Wnt/β-catenina y Notch puede contribuir aún más a la patogenia tumoral desmoide.17
- La desregulación de la vía Wnt/β-catenina se ha relacionado con la patogénesis de los tumores desmoides2,24
- La acumulación nuclear de β-catenina y la subsiguiente transcripción génica son un factor clave que impulsa la proliferación de células tumorales desmoides2,25
- La acumulación nuclear de β-catenina puede iniciarse por2,25
- Mutaciones activadoras del gen de la β-catenina CTNNB1
- Mutaciones inactivadoras en el APC regulador negativo, a menudo en poliposis adenomatosa familiar (PAF)
- La vía Notch puede estar activa en los tumores desmoides26
- Cuando se desregula, Notch puede activar vías que contribuyen al crecimiento tumoral26
- La señalización del receptor Notch requiere la activación proteolítica por la enzima γ-secretasa26
- La escisión de la γ-secretasa libera el dominio intracelular de Notch (DICN), que se transloca al núcleo y activa la transcripción génica26
- La interferencia entre las vías Wnt/β-catenina y Notch puede contribuir aún más a la patogenia tumoral desmoide.18
Riesgo de recidiva
- Las tasas de recidiva pueden verse influidas por la localización del tumor:17
- Se cree que los tumores de las extremidades son localmente agresivos y tienen tasas de recidiva que van del 24 % al 77 %
- Las tasas de recidiva local de tumores intraabdominales en pacientes con PAF son superiores a las de los tumores extraabdominales y se notificó que eran del 57 % al 86 %
Existe un alto riesgo de recidiva local después de la cirugía17
- Las tasas de recidiva pueden exacerbarse por traumatismos, como traumatismos quirúrgicos, y oscilan aproximadamente entre el 25 % y el 60 % a los 5 años17
- La invasión de los principales vasos y nervios y la calidad de los bordes quirúrgicos son factores clave para la elevada tasa de recidiva posoperatoria26
- Desafortunadamente, incluso cuando los bordes quirúrgicos no presentan tumores, las tasas de recidiva son altas27
- El hecho de que algunos tumores reaparecieron después de la cirugía pero luego permanecieron estables sin tratamiento indica que los factores de crecimiento liberados después de la cirugía pueden haber fomentado la recidiva en tumores que de otro modo habrían sido de escasa malignidad5
- La mutación específica S45F en el gen CTNNB1 parece estar asociada con una peor supervivencia sin recidiva después de la cirugía, tal como han sugerido múltiples cohortes retrospectivas28
- La supervivencia sin recidiva a los 5 años fue significativamente menor en pacientes con tumores desmoides que portaban la mutación S45F (p < 0,0001) en comparación con pacientes con tumores con la mutación T41A o sin mutación29. Dado que estos resultados proceden de estudios observacionales, es importante interpretarlos considerando la variabilidad entre cohortes y factores como el sitio tumoral y el manejo aplicado.
| MUTACIÓN | SUPERVIVENCIA LIBRE DE RECURRENCIA ESTIMADA (IC 95%) |
|---|---|
| 45F | 23% (10%-40%) |
| 41A | 57% (43%-69%) |
| CTNNB1 non mutado | 65% (38%-83%) |
Los pacientes con mutaciones en CTNNB1 en el codón 45 (45F) presentaron un riesgo 3 veces mayor de recidiva después de la cirugía29
En un metanálisis, se notificó que el tamaño del tumor era un mediador importante del aumento del riesgo de recidiva en pacientes con la mutación S45F en el gen CTNNB1.30
Principios de la gestión
Es imprescindible seleccionar cuidadosamente la estrategia de tratamiento para cada paciente con tumores desmoides para optimizar el control tumoral y mejorar la calidad de vida18
En la última década se han realizado esfuerzos importantes para estandarizar el tratamiento de esta enfermedad.18
Actualmente, las necesidades no cubiertas en los tumores desmoides incluyen un diagnóstico temprano y preciso y tratamientos aprobados indicados para pacientes con tumores desmoides.17
En un estudio realizado en el Memorial Sloan Kettering Cancer Center, el 58 % de los pacientes con tumores desmoides pasaron de vigilancia activa a tratamiento de primera línea sin progresión radiográfica del tumor.31†
Los objetivos del tratamiento no deben centrarse únicamente en los marcadores clínicos, como la supervivencia sin progresión, sino también considerar los criterios de valoración relevantes para el paciente, como la reducción de la carga de síntomas específicos del tumor desmoide (por ejemplo, el dolor) y su impacto en la vida de los pacientes, la mejora del funcionamiento en las actividades diarias y la calidad de vida en general.17
Identificación temprana de la progresión
La identificación de la progresión del tumor desmoide puede dar lugar al inicio oportuno del tratamiento adecuado32,33
- Para ayudar a mejorar los resultados de los pacientes, los profesionales sanitarios deben evaluar la progresión lo antes posible con al menos uno de los siguientes:
- El dolor puede ser un indicador pronóstico de progresión34 y puede asociarse a peores resultados35
- El riesgo de progresión puede ser mayor para tumores más grandes3,33
†Los pacientes con tumores desmoides primarios o recidivantes (n = 160) se identificaron de forma retrospectiva a partir de una base de datos institucional. Entre los pacientes en observación inicial para los que se disponía de RM seriadas, 14 de 24 (58 %) de los que se sometieron a tratamiento activo no experimentaron crecimiento tumoral según los criterios RECIST.31 Elaborado a partir del texto, referencia 31.
Escuche las perspectivas de un oncólogo médico sobre los tumores desmoides
Comprender los tumores desmoides
Vea cómo el Dr. Riedel, oncólogo médico del Duke Health y Duke Cancer Institute, proporciona una visión general de los tumores desmoides, incluida su fisiopatología, presentaciones clínicas e impacto en los pacientes.
APC, gen Adenomatosis Polyposis Coli; TAC, tomografía computarizada; CTNNB1, gen de la β-catenina 1; PAF, poliposis adenomatosa familiar; RM, resonancia magnética; DICN, dominio intracelular de Notch; RECIST, Criterios de evaluación de la respuesta en tumores sólidos; S45F, tipo de mutación; T41A, tipo de mutación; Wnt, sitio de integración relacionado con Wingless.
Referencias
- Kasper B et al. Desmoid Working Group. An update on the management of sporadic desmoid-type fibromatosis: a European Consensus Initiative between Sarcoma Patients EuroNet (SPAEN) and European Organization for Research and Treatment of Cancer (EORTC)/Soft Tissue and Bone Sarcoma Group (STBSG). Ann Oncol. 2017;28(10):2399-2408. doi: 10.1093/annonc/mdx323.
- Penel N et al. Adult desmoid tumors: biology, management and ongoing trials. Curr Opin Oncol. 2017;29(4):268-274. doi: 10.1097/CCO.0000000000000374.
- Gronchi A et al. Desmoid tumor working group. The management of desmoid tumours: a joint global consensus-based guideline approach for adult and paediatric patients. Eur J Cancer. 2020;127:96-107. doi: 10.1016/j.ejca.2019.11.013.
- Joglekar SB et al. Current perspectives on desmoid tumors: the mayo clinic approach. Cancers (Basel). 2011;3(3):3143-3155. doi: 10.3390/cancers3033143.
- Bonvalot S et al. The treatment of desmoid tumors: a stepwise clinical approach. Ann Oncol. 2012;23(suppl 10):x158-x166. doi: 10.1093/annonc/mds298.
- Constantinidou A et al. Clinical presentation of desmoid tumors. En: Litchman C, ed. Desmoid Tumors. Springer; 2012:cap. 2. Consultado el 9 de abril de 2024. https://www.researchgate.net/publication/226455135. doi: 10.1007/978-94-007-1685-8_2
- Penel N et al. Surgical versus non-surgical approach in primary desmoid-type fibromatosis patients: a nationwide prospective cohort from the French Sarcoma Group. Eur J Cancer. 2017;83:125-131. doi: 10.1016/j.ejca.2017.06.017.
- Shinagare AB et al. A to Z of desmoid tumors. AJR Am J Roentgenol. 2011;197(6):W1008-W1014. doi: 10.2214/AJR.11.6657.
- Koshariya M et al. Giant desmoid tumor of the anterior abdominal wall in a young female: a case report. Case Rep Surg. 2013;2013:780862. doi: 10.1155/2013/780862.
- McDonald ES et al. Best cases from the AFIP: extraabdominal desmoid-type fibromatosis. Radiographics. 2008;28(3):901-906. doi: 10.1148/rg.283075169.
- Abrão FC et al. Desmoid tumors of the chest wall: surgical challenges and possible risk factors. Clinics (Sao Paulo). 2011;66(4):705-708. doi: 10.1590/s1807-59322011000400028.
- Xie Y et al. Recurrent desmoid tumor of the mediastinum: a case report. Oncol Lett. 2014;8(5):2276-2278. doi: 10.3892/ol.2014.2431.
- Scaramussa FS et al. Desmoid tumor in hand: a case report. SM J Orthop. 2016;2(3):1036.
- Baranov E et al. Soft tissue special issue: fibroblastic and myofibroblastic neoplasms of the head and neck. Head Neck Pathol. 2020;14(1):43-58. doi: 10.1007/s12105-019-01104-3.
- Ingley KM et al. High prevalence of persistent emotional distress in desmoid tumor. Psychooncology. 2020;29(2):311-320. doi: 10.1002/pon.5250.
- Gounder MM et al. Prospective development of a patient-reported outcomes instrument for desmoid tumors or aggressive fibromatosis. Cancer. 2020;126(3):531-539. doi: 10.1002/cncr.32555.
- Bektas M et al. Desmoid tumors: a comprehensive review. Adv Ther. 2023;40(9):3697-3722. doi: 10.1007/s12325-023-02592-0.
- Kasper B et al. Desmoid Tumor Working Group. Current management of desmoid tumors: a review. JAMA Oncol. 2024;10(8):1121-1128. doi: 10.1001/jamaoncol.2024.1805.
- Ravi V et al. Desmoid tumors: epidemiology, molecular pathogenesis, clinical presentation, diagnosis, and local therapy Jun 2024 UptoDate.
- Skubitz KM. Biology and treatment of aggressive fibromatosis or desmoid tumor. Mayo Clin Proc. 2017;92(6):947-964. doi: 10.1016/j.mayocp.2017.02.012.
- Lopez R et al. Problems in diagnosis and management of desmoid tumors. Am J Surg. 1990;159(5):450-453. doi: 10.1016/s0002-9610(05)81243-7.
- Kasper B et al. Desmoid tumors: clinical features and treatment options for advanced disease. Oncologist. 2011;16(5):682-93. doi: 10.1001/jamaoncol.2024.1805.
- Crago AM et al. Near universal detection of alterations in CTNNB1 and Wnt pathway regulators in desmoid-type fi bromatosis by whole-exome sequencing and genomic analysis. Genes Chromosomes Cancer. 2015;54(10):606-615. doi: 10.1002/gcc.22272.
- Gronchi A et al. Desmoid tumor working group. The management of desmoid tumours: a joint global consensus-based guideline approach for adult and paediatric patients [supplementary appendix]. Eur J Cancer. 2020;127:96-107. doi: 10.1016/j.ejca.2019.11.013.
- Shang H et al. Targeting the Notch pathway: a potential therapeutic approach for desmoid tumors. Cancer. 2015;121(22):4088-4096. doi: 10.1002/cncr.29564.
- Wang YF et al. Postoperative recurrence of desmoid tumors: clinical and pathological perspectives. World J. Surg Oncol. 2015;13:26. doi: 10.1186/s12957-015-0450-8.
- Easter DW et al. Recent trends in the management of desmoid tumors. Summary of 19 cases and review of the literature. Ann Surg. 1989;210(6):765-769. doi: 10.1097/00000658-198912000-00012.
- Napolitano A et al. Recent advances in desmoid tumor therapy. Cancers (Basel). 2020;12(8):2135. doi: 10.3390/cancers12082135.
- Lazar AJ et al. Specific mutations in the beta-catenin gene (CTNNB1) correlate with local recurrence in sporadic desmoid tumors. Am J Pathol. 2008;173(5):1518-27. doi: 10.2353/ajpath.2008.080475.
- Timbergen MJM et al. The prognostic role of β-Catenin mutations in desmoid-type fibromatosis undergoing resection only: a meta-analysis of individual patient data. Ann Surg. 2021;273(6):1094-1101. doi: 10.1097/SLA.0000000000003698.
- Cassidy MR et al. Association of MRI T2 signal intensity with desmoid tumor progression during active observation: a retrospective cohort study. Ann Surg. 2020;271(4):748-755. doi: 10.1097/SLA.0000000000003073.
- Tomado como referencia con permiso de NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines®) for Soft Tissue Sarcoma V.1.2024. © National Comprehensive Cancer Network, Inc. 2024. Todos los derechos reservados. Consultado el 29 de abril de 2024. Para ver la versión más reciente y completa de las directrices, visite NCCN.org. La NCCN no ofrece ninguna garantía de ningún tipo en relación con su contenido, uso o aplicación y rechaza cualquier responsabilidad sobre su aplicación o uso de cualquier forma.
- Kasper B et al. Desmoid Tumor Working Group. Current management of desmoid tumors: a review. [supplementary appendix] JAMA Oncol. 2024;10(8):1121-1128. doi: 10.1001/jamaoncol.2024.1805.
- Cuomo P et al. Extra-abdominal desmoid tumor fibromatosis: a multicenter EMSOS study. BMC Cancer. 2021;21(1):437. doi: 10.1186/s12885-021-08189-6.
- Penel N et al. Pain in desmoid-type fibromatosis: prevalence, determinants and prognosis value. Int J Cancer. 2023;153(2):407-416. doi: 10.1002/ijc.34493.