Informazioni sui tumori desmoidi
Panoramica della malattia
Una malattia infiltrante e aggressiva1
- I tumori desmoidi sono tumori localmente aggressivi dei tessuti molli, potenzialmente associati a morbilità, con tendenza a infiltrare le strutture circostanti e a diffondersi lungo le fasce e i muscoli1,2
- A volte indicati come fibromatosi aggressiva o fibromatosi desmoide,3 questi tumori mesenchimali possono essere gravi, debilitanti e, in rari casi, causare persino danni potenzialmente letali agli organi 2
- I tumori desmoidi possono infiltrare i tessuti adiacenti comprimendo muscoli, nervi e vasi4.5
Sintomatologia e sedi tumorali
I tumori desmoidi possono causare morbilità gravi e debilitanti2
- La sintomatologia correlata ai tumori desmoidi varia in base alla sede dell’insorgenza tumorale5.6
- Uno studio di coorte prospettico ha evidenziato che i tumori della parete toracica, degli arti superiori e della testa e del collo sono associati a esiti sfavorevoli dopo l’intervento chirurgico7
| SEDE DEL TUMORE | FREQUENZA STIMATA5 | SINTOMI E COMPLICANZE COMUNI |
|---|---|---|
| Intra-addominale (incluso il mesentere) | 20% | La compressione può causare dolore, cachessia, malessere, distensione addominale o ostruzione dell’intestino o degli ureteri5,8 |
| Parete addominale | 16% | I tumori di grandi dimensioni possono causare stiramento dei tessuti, compressione dei vasi sanguigni e spostamento dell’intestino o della vescica9 |
| Arti inferiori | 16% | Mobilità limitata, dolore, rigidità muscolare o deformità5,10 |
| Parete toracica | 15% | Dispnea,5 disfagia,5 invasione pleurica,8 coinvolgimento della colonna vertebrale11 o delle coste,12 erosione ossea,12 e dolore12 |
| Arti superiori | 14% | Mobilità ridotta, coinvolgimento di muscoli e legamenti, debolezza dell’arto, deformità o dolore5,13 |
| Testa e Collo | 8% | Dolore, deficit neurologici, prossimità a strutture vitali, incluso il rischio di morte per compromissione vascolare o delle vie aeree14 |
| Altro | 11% | Sintomi e complicanze dipendenti dalla sede5,6 |
La posizione dei tumori desmoidi può influire significativamente sulla qualità della vita.15 Per esempio, un tumore desmoide con neoformazioni “a viticcio”1, che avvolgono i nervi, può essere associato a dolore neuropatico debilitante.5.16
Decorso della malattia
Variabile e imprevedibile1
- I tumori desmoidi sono caratterizzati da un decorso della malattia variabile e imprevedibile a seconda della sede del tumore e della morbilità associata1.5
- Circa il 50% dei tumori desmoidi mostra una biologia aggressiva continuando a crescere o diventando sintomatico. La grande maggioranza delle progressioni (89%) si verifica entro i primi 2 anni di osservazione4
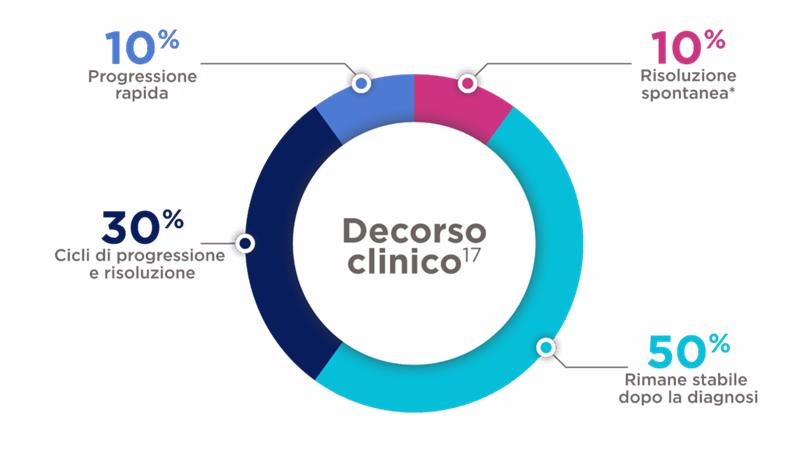
Decorso clinico dei tumori desmoidi
*Il 10-28% dei tumori desmoidi si risolverà spontaneamente senza trattamento17
Incidenza e fattori di rischio
Epidemiologia
Il tumore desmoide ha un’incidenza di circa 5 casi per 1 milione di popolazione all’anno.18
L'Orphanet Report Series indica un’incidenza annuale media di 3 casi di tumori desmoidi per milione di anni-persona in Europa.17
Gli studi epidemiologici rivelano che la maggior parte dei casi di tumore desmoide compare nella fascia di età compresa tra i 20 e i 44 anni.17
- I tumori desmoidi sono rari nei giovani e negli anziani19
- La stima dell’incidenza è aumentata negli anni più recenti, il che potrebbe essere correlato a un miglioramento delle tecniche diagnostiche17
Sesso femminile
Il rapporto donne-uomini è di circa 2-3:1,20
- La gravidanza può favorire lo sviluppo di tumori desmoidi4
Trauma precedente
Circa il 25% dei pazienti con tumori desmoidi presenta un’anamnesi di precedente trauma.5
- Lesioni o interventi chirurgici possono aumentarne il rischio21
Mutazioni del gene APC(adenomatous polyposis coli, gene della poliposi adenomatosa del colon)
Le caratteristiche fenotipiche sono correlate alla posizione della mutazione APC rispetto a determinati codoni.22
- I pazienti con poliposi adenomatosa familiare (familial adenomatous polyposis, FAP) presentano un rischio 1.000 volte maggiore di sviluppare tumori desmoidi rispetto alla popolazione generale20
Eziologia e patogenesi dei tumori desmoidi
La comprensione della patogenesi molecolare è di notevole interesse in questa malattia a causa dell'elevata variabilità del suo decorso clinico19
L’eziologia dei tumori desmoidi non è nota. Tuttavia, l’identificazione di alterazioni cromosomiche clonali in una percentuale significativa di casi supporta la natura neoplastica di questi tumori.19
- Si ritiene che la patogenesi dei tumori desmoidi sia collegata a traumi
- l’intervento chirurgico può talvolta favorire la crescita del tumore.4
- I fattori di crescita rilasciati dopo l’intervento chirurgico, durante la fase iniziale della guarigione della ferita, potrebbero trasmettere segnali che promuovono l’attivazione della β-catenina4
- La gravidanza può promuovere il tumore desmoide non solo a causa di effetti ormonali, ma anche a causa del rilascio sistemico di fattori di crescita4
- Sono stati implicati due pathway nel pathway canonico Wnt/β-catenina/APC, in cui le mutazioni del gene CTNNB1 o del gene APC portano all’accumulo di β-catenina e nel pathway Notch, in cui si verificano due scissioni dei recettori Notch 17
- Si ritiene che nella patogenesi dei tumori desmoidi siano coinvolte la potenziale interferenza tra il pathway Notch e Wnt, così come l’attivazione del pathway Notch derivante dalla disregolazione del pathway Wnt.17
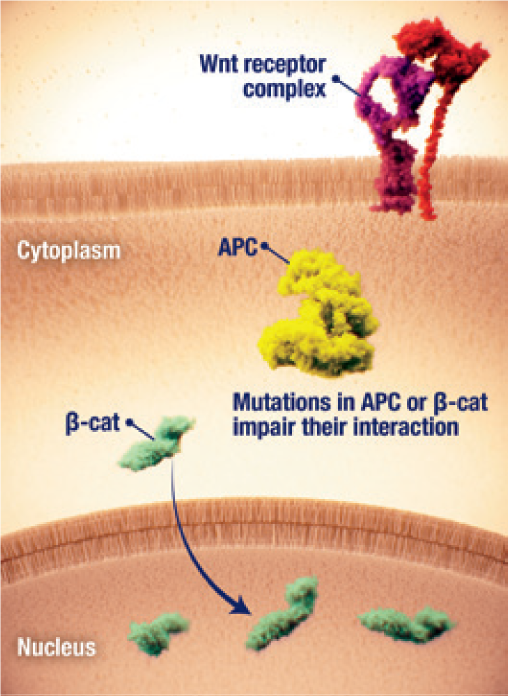
Accumulo nucleare di β-catenina
- La disregolazione del pathway Wnt/β-catenina è stata implicata nella patogenesi dei tumori desmoidi2,23
- L’accumulo nucleare di β-catenina e la trascrizione del gene a valle sono fattori chiave della proliferazione delle cellule tumorali desmoidi2,24
- L’accumulo nucleare di β-catenina può essere avviato da2,24
- Mutazioni attivanti del gene della β-catenina CTNNB1
- Mutazioni inattivanti del gene onco-soppressore APC, spesso riscontrate nella poliposi adenomatosa familiare (FAP)
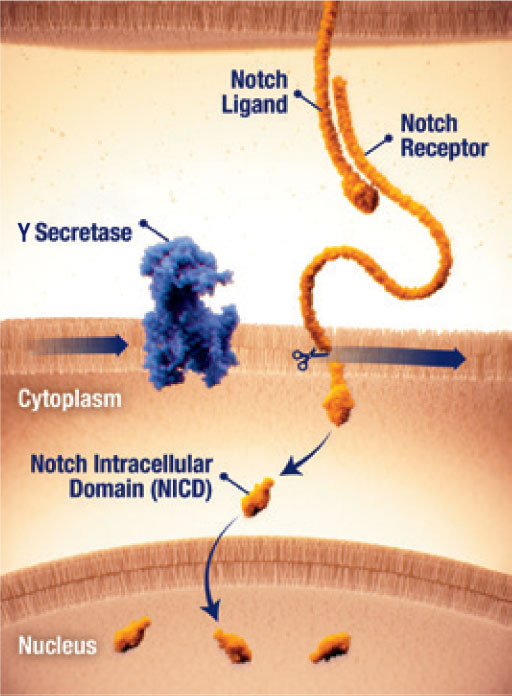
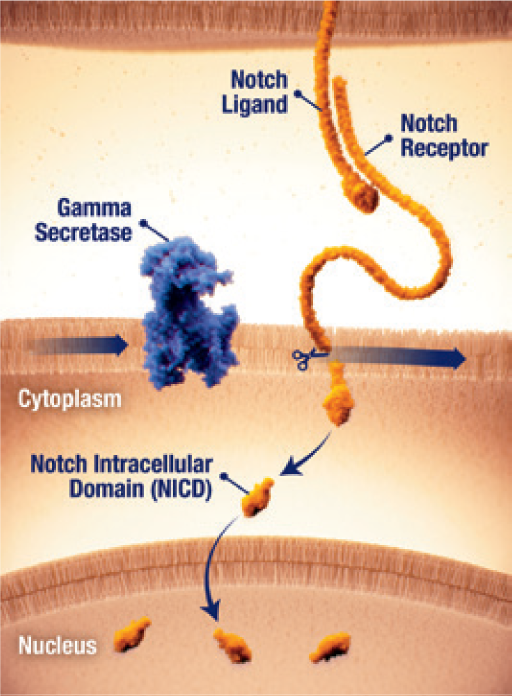
Attivazione di Notch da parte della γ-secretasi
- Il pathway di Notch può essere attivo nei tumori desmoidi25
- Quando disregolato, Notch può attivare una trasmissione di segnali che contribuiscono alla crescita tumorale25
- La trasmissione dei segnali del recettore di Notch richiede l’attivazione proteolitica da parte dell’enzima γ-secretasi (gamma secretasi)25
- Il clivaggio della γ-secretasi rilascia il dominio intracellulare Notch (Notch intracellular domain, NICD) che trasloca nel nucleo e attiva la trascrizione genica25
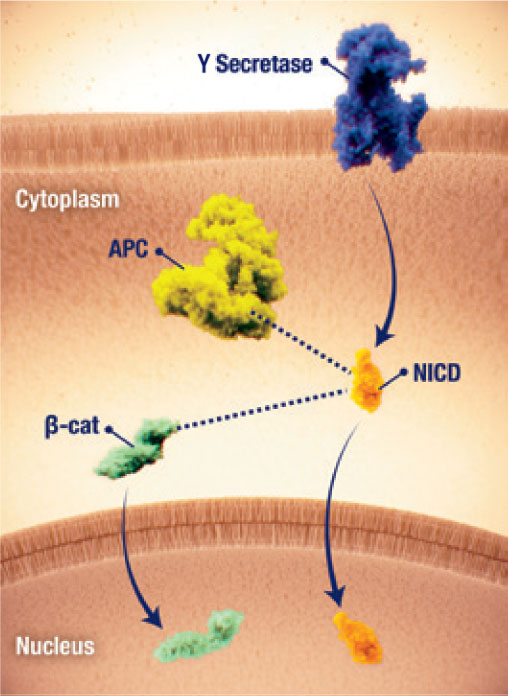
Interazione dei pathway
- L’interazione tra il pathway di Wnt/β-catenina e di Notch può contribuire ulteriormente alla patogenesi del tumore desmoide17
- La disregolazione del pathway Wnt/β-catenina è stata implicata nella patogenesi dei tumori desmoidi2,24
- L’accumulo nucleare di β-catenina e la trascrizione del gene a valle sono fattori chiave della proliferazione delle cellule tumorali desmoidi2,25
- L’accumulo nucleare di β-catenina può essere avviato da2,25
- Mutazioni attivanti del gene della β-catenina CTNNB1
- Mutazioni inattivanti nel regolatore negativo APC, spesso nella poliposi adenomatosa familiare (FAP)
- Il pathway di Notch può essere attivo nei tumori desmoidi26
- Quando disregolato, Notch può attivare vie che contribuiscono alla crescita tumorale26
- La segnalazione del recettore Notch richiede l’attivazione proteolitica da parte dell’enzima γ-secretasi26
- Il clivaggio della γ-secretasi rilascia l’NICD che si trasloca nel nucleo e attiva la trascrizione genica26
- L’interazione tra il pathway di Wnt/β-catenina e di Notch può contribuire ulteriormente alla patogenesi del tumore desmoide18
Rischio di recidiva
- I tassi di recidiva possono essere influenzati dalla sede del tumore:17
- Si ritiene che i tumori localizzati negli arti siano localmente aggressivi e presentino tassi di recidiva compresi tra il 24% e il 77%
- I tassi di recidiva locale dei tumori intra-addominali nei pazienti con FAP sono superiori a quelli dei tumori extra-addominali e sono compresi tra il 57% e l’86%
Esiste un alto rischio di recidiva locale dopo l’intervento chirurgico17
- I tassi di recidiva possono essere esacerbati da un trauma, come il trauma chirurgico, e variano da circa il 25% al 60% a 5 anni17
- L’invasione dei principali vasi e nervi e la qualità dei margini chirurgici sono fattori chiave per l’elevato tasso di recidiva postoperatoria26
- Purtroppo, anche quando i margini chirurgici sono privi di tumore, i tassi di recidiva sono elevati27
I fattori di crescita rilasciati dopo l’intervento chirurgico durante la fase iniziale di guarigione della ferita potrebbero promuovere l’attivazione della β-catenina.4
- Il fatto che alcuni tumori siano recidivati dopo l’intervento chirurgico, ma che in seguito siano rimasti stabili senza trattamento, suggerisce che i fattori di crescita rilasciati dopo l’intervento chirurgico potrebbero aver favorito la recidiva nei tumori che altrimenti sarebbero stati indolenti4
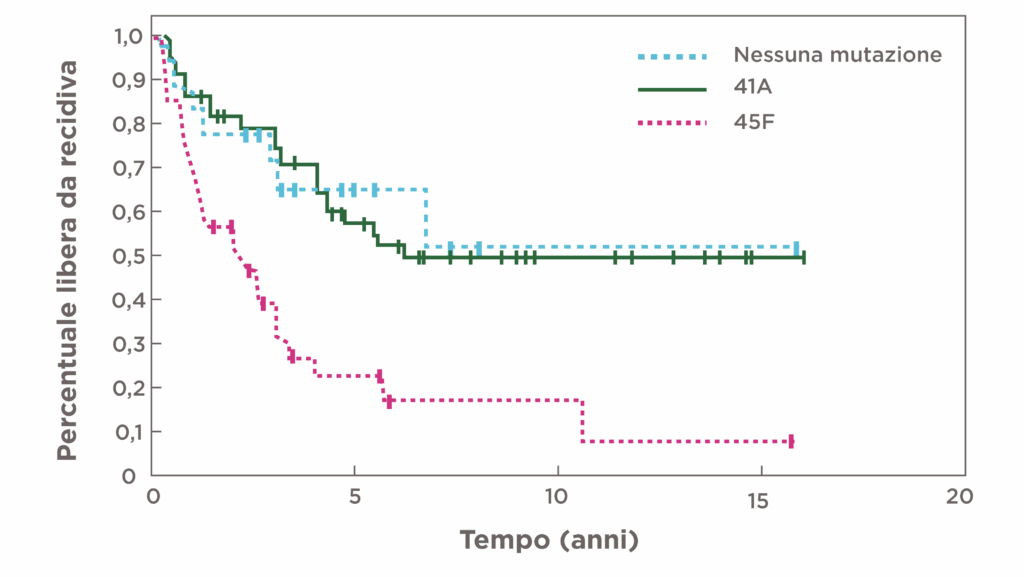
- La mutazione specifica di CTNNB1 S45F sembra essere associata a una peggiore sopravvivenza libera da recidiva dopo l’intervento chirurgico28
- La sopravvivenza libera da recidiva a 5 anni era significativamente più scarsa nei pazienti con tumori desmoidi S45F-mutati (P<0,0001) rispetto ai pazienti con mutazione T41A o con tumori non mutati29
| MUTAZIONE | SOPRAVVIVENZA LIBERA DA RECIDIVA STIMATA (IC 95%)(95% CI) |
|---|---|
| 45F | 23% (10%-40%) |
| 41A | 57% (43%-69%) |
| CTNNB1 non mutato | 65% (38%-83%) |
I pazienti con mutazioni di CTNNB1 a livello del codone 45 (45F) presentavano un rischio 3 volte maggiore di recidiva dopo l’intervento chirurgico29
In una metanalisi è stato riportato che le dimensioni del tumore sono un importante mediatore per un aumento del rischio di recidiva nei pazienti con mutazione CTNNB1 S45F.30
Principi di gestione
È fondamentale scegliere attentamente la strategia di gestione per ciascun paziente affetto da tumori desmoidi per ottimizzare il controllo del tumore e migliorare la qualità della vita18
Nell’ultimo decennio sono stati compiuti importanti sforzi per standardizzare la gestione di questa malattia.18
Attualmente, le esigenze insoddisfatte nell’ambito dei tumori desmoidi includono una diagnosi precoce e accurata e trattamenti approvati indicati per i/le pazienti con tumori desmoidi.17
In uno studio condotto presso il Memorial Sloan Kettering Cancer Center, il 58% dei pazienti con tumori desmoidi è passato dalla sorveglianza attiva al trattamento di prima linea senza progressione radiografica del tumore.31†
Gli obiettivi del trattamento non devono concentrarsi esclusivamente sui marcatori clinici, come la sopravvivenza libera da progressione, ma devono anche considerare gli endpoint rilevanti per il paziente, come una riduzione del carico dei sintomi specifici del tumore desmoide (per es., dolore) e il suo impatto sulla vita dei pazienti, il miglioramento delle attività quotidiane e la qualità della vita complessiva.17
Identificazione precoce della progressione
L’identificazione della progressione del tumore desmoide può portare a un avvio tempestivo del trattamento appropriato
- Per aiutare a migliorare gli esiti dei pazienti, gli operatori sanitari devono valutare la progressione il prima possibile con almeno uno dei seguenti metodi:
- Il dolore può essere un indicatore prognostico di progressione34 e può essere associato a esiti peggiori35
- Il rischio di progressione può essere maggiore per i tumori più grandi3,33
†I pazienti con tumori desmoidi primari o ricorrenti (n=160) sono stati identificati retrospettivamente da una banca dati istituzionale. Tra i pazienti sottoposti a osservazione iniziale per i quali erano disponibili RM seriali, 14 su 24 (58%) sottoposti a trattamento attivo non hanno manifestato crescita tumorale secondo i criteri RECIST.31 Elaborato dal testo, riferimento 31.
Ascolta i punti di vista di un oncologo medico sui tumori desmoidi
Comprendere i tumori desmoidi
Osservare il Dott. Riedel, medico oncologo del Duke Health and Duke Cancer Institute, mentre fornisce una panoramica dei tumori desmoidi che include fisiopatologia, presentazioni cliniche e impatto sui/sulle pazienti.
APC, gene della poliposi da adenomatosi del colon; TC, tomografia computerizzata; CTNNB1, gene della catenina β1; FAP, poliposi adenomatosa familiare; RM, risonanza magnetica per immagini; NICD, Notch IntraCellular Domain; RECIST, Criteri di valutazione della risposta nei tumori solidi; S45F, tipo di mutazione; T41A, tipo di mutazione; Wnt, sito di integrazione correlato a Wingless.
Riferimenti
- Kasper B et al. Desmoid Working Group. An update on the management of sporadic desmoid-type fibromatosis: a European Consensus Initiative between Sarcoma Patients EuroNet (SPAEN) and European Organization for Research and Treatment of Cancer (EORTC)/Soft Tissue and Bone Sarcoma Group (STBSG). Ann Oncol. 2017;28(10):2399-2408.
- Penel N et al. Adult desmoid tumors: biology, management and ongoing trials. Curr Opin Oncol. 2017;29(4):268-274.
- Gronchi A et al. Desmoid tumor working group. The management of desmoid tumours: a joint global consensus-based guideline approach for adult and paediatric patients. Eur J Cancer. 2020; 127: 96-107.
- Bonvalot S et al. The treatment of desmoid tumors: a stepwise clinical approach. Ann Oncol. 2012;23(suppl 10):x158-x166.
- Constantinidou A et al. Clinical presentation of desmoid tumors. In: Litchman C, ed. Desmoid Tumors. Springer; 2012:chap 2. Accesso 9 aprile 2024. https://www.researchgate.net/publication/226455135.
- Joglekar SB et al. Current perspectives on desmoid tumors: the mayo clinic approach. Cancers (Basel). 2011;3(3):3143-3155.
- Penel N et al. Surgical versus non-surgical approach in primary desmoid-type fibromatosis patients: a nationwide prospective cohort from the French Sarcoma Group. Eur J Cancer. 2017;83:125-131.
- Shinagare AB et al. A to Z of desmoid tumors. AJR Am J Roentgenol. 2011;197(6):W1008-W1014.
- Koshariya M et al. Giant desmoid tumor of the anterior abdominal wall in a young female: a case report. Case Rep Surg. 2013; 2013:780862.
- McDonald ES et al. Best cases from the AFIP: extraabdominal desmoid-type fibromatosis. Radiographics. 2008;28(3):901-906.
- Abrão FC et al. Desmoid tumors of the chest wall: surgical challenges and possible risk factors. Clinics (Sao Paulo). 2011;66(4):705-708.
- Xie Y et al. Recurrent desmoid tumor of the mediastinum: a case report. Oncol Lett. 2014;8(5):2276-2278.
- Scaramussa FS et al. Desmoid tumor in hand: a case report. SM J Orthop. 2016;2(3):1036.
- Baranov E et al. Soft tissue special issue: fibroblastic and myofibroblastic neoplasms of the head and neck. Head Neck Pathol. 2020;14(1):43-58.
- Ingley KM et al. High prevalence of persistent emotional distress in desmoid tumor. Psychooncology. 2020;29(2):311-320.
- Gounder MM et al. Prospective development of a patient-reported outcomes instrument for desmoid tumors or aggressive fibromatosis. Cancer. 2020;126(3):531-539.
- Bektas M et al. Desmoid tumors: a comprehensive review. Adv Ther. 2023;40(9):3697-3722.
- Kasper B et al. Desmoid Tumor Working Group. Current management of desmoid tumors: a review. JAMA Oncol. 2024;10(8):1121-1128.
- Ravi V et al. Desmoid tumors: epidemiology, molecular pathogenesis, clinical presentation, diagnosis, and local therapy Jun 2024 UptoDate.
- Skubitz KM. Biology and treatment of aggressive fibromatosis or desmoid tumor. Mayo Clin Proc. 2017;92(6):947-964.
- Lopez R et al. Problems in diagnosis and management of desmoid tumors. Am J Surg. 1990;159(5):450-453.
- Kasper B et al. Desmoid tumors: clinical features and treatment options for advanced disease. Oncologist. 2011;16(5):682-93.
- Crago AM et al. Near universal detection of alterations in CTNNB1 and Wnt pathway regulators in desmoid-type fi bromatosis by whole-exome sequencing and genomic analysis. Genes Chromosomes Cancer. 2015;54(10):606-615.
- Gronchi A et al. Desmoid Tumor Working Group. The management of desmoid tumours: a joint global consensus-based guideline approach for adult and paediatric patients [supplementary appendix]. Eur J Cancer. 2020; 127: 96-107.
- Shang H et al. Targeting the Notch pathway: a potential therapeutic approach for desmoid tumors. Cancer. 2015;121(22):4088-4096.
- Wang YF et al. Postoperative recurrence of desmoid tumors: clinical and pathological perspectives. World J Surg Oncol. 2015;13:26.
- Easter DW et al. Recent trends in the management of desmoid tumors. Summary of 19 cases and review of the literature. Ann Surg. 1989;210(6):765-769.
- Napolitano A et al. Recent advances in desmoid tumor therapy. Cancers (Basel). 2020;12(8):2135.
- Lazar AJ et al. Specific mutations in the beta-catenin gene (CTNNB1) correlate with local recurrence in sporadic desmoid tumors. Am J Pathol. 2008;173(5):1518-27.
- Timbergen MJM et al. The prognostic role of β-Catenin mutations in desmoid-type fibromatosis undergoing resection only: a meta-analysis of individual patient data. Ann Surg. 2021;273(6):1094-1101.
- Cassidy MR et al. Association of MRI T2 signal intensity with desmoid tumor progression during active observation: a retrospective cohort study. Ann Surg. 2020;271(4):748-755.
- Citato con l’autorizzazione delle NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines®) per il sarcoma dei tessuti molli V.1.2024. © National Comprehensive Cancer Network, Inc. 2024. Tutti i diritti riservati. Accesso 29 aprile 2024. Per visualizzare la versione più recente e completa delle linee guida, visita il sito NCCN.org. NCCN non fornisce alcuna garanzia di alcun tipo in merito al loro contenuto, utilizzo o applicazione e declina qualsiasi responsabilità per la loro applicazione o il loro utilizzo in qualsiasi modo.
- Kasper B et al. Desmoid Tumor Working Group. Current management of desmoid tumors: a review. [supplementary appendix] JAMA Oncol. 2024;10(8):1121-1128.
- Cuomo P et al. Extra-abdominal desmoid tumor fibromatosis: a multicenter EMSOS study. BMC Cancer. 2021;21(1):437.
- Penel N et al. Pain in desmoid-type fibromatosis: prevalence, determinants and prognosis value. Int J Cancer. 2023;153(2):407-416.